Receita Federal retém carga de medicamento avaliada em R$ 1 milhão no Aeroporto Internacional do Recife
Passageiro estava transportando canetas do remédio Mounjaro de forma irregular. Ele foi abordado em fiscalização rotineira quando chegava ao Recife

Clique aqui e escute a matéria
Aproximadamente R$ 1 milhão em carga de medicamento foram retidos no Aeroporto Internacional do Recife na madrugada deste domingo (13). A ação foi realizada pela Inspetoria da Receita Federal e apreendeu 389 canetas do remédio Mounjaro.
O passageiro estava transportando os itens de forma irregular do Reino Unido e foi abordado em uma fiscalização rotineira de controle no momento em que chegava à capital pernambucana.
A retenção pela Receita Federal busca combater os crimes de contrabando e descaminho para garantir a segurança e legalidade no comércio internacional.
Além de grande quantidade, a carga estava sem receita médica ou autorização da Agência Nacional de Vigilância Sanitária (Anvisa).
De acordo com a Receita Federal, a importação de medicamentos “deve seguir rigorosamente a legislação vigente, incluindo a apresentação de documentos específicos, como receita médica e autorização da Anvisa, quando aplicável”.
Mounjaro
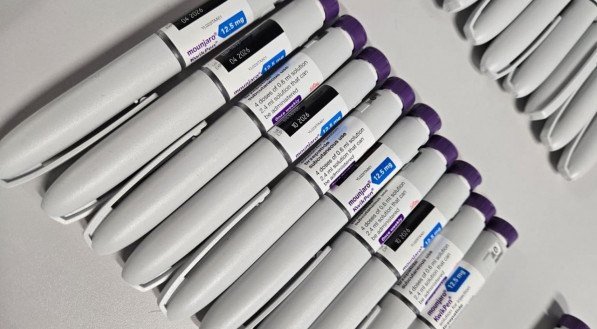
Mounjaro deve ser lançado oficialmente no Brasil no mês de junho - Divulgação
O Mounjaro é um medicamento da farmacêutica Eli Lilly e deve ser lançado oficialmente no Brasil no mês de junho. O remédio é manipulado ou alternativo para o tratamento do diabetes tipo 2. Assim como o concorrente Ozempic, ele tem como efeito a perda de peso.
Após chegar ao Brasil, medicamento será vendido em canetas injetáveis, com aplicação semanal das doses. O preço máximo foi fixado em R$ 3.627,82 para um mês de tratamento.
Em fevereiro deste ano, Sociedade Brasileira de Endocrinologia e Metabologia (Sbem), a Sociedade Brasileira de Diabetes (SBD) e a Associação Brasileira para o Estudo da Obesidade e Síndrome Metabólica (Abeso) emitiram um alerta sobre os riscos do uso de injetáveis como este.
Além de chamar atenção para a dosagem, indicando que "há relatos documentados por órgãos internacionais, como a FDA (Food and Drug Administration), de problemas graves, incluindo contaminação, substituição por outros compostos e variação perigosa da dosagem", as entidades destacaram a comercialização irregular dos medicamentos.
As sociedades médicas cobraram, ainda, a fiscalização de órgãos reguladores, como a Anvisa e os Conselhos de Medicina.
"A Sbem, a SBD e a Abeso reforçam que o uso seguro desses medicamentos deve ser feito apenas sob prescrição e com acompanhamento médico, sempre com produtos devidamente regulamentados", destaca o alerta.

